炭酸 イオン解離式 839810-炭酸 イオン解離式
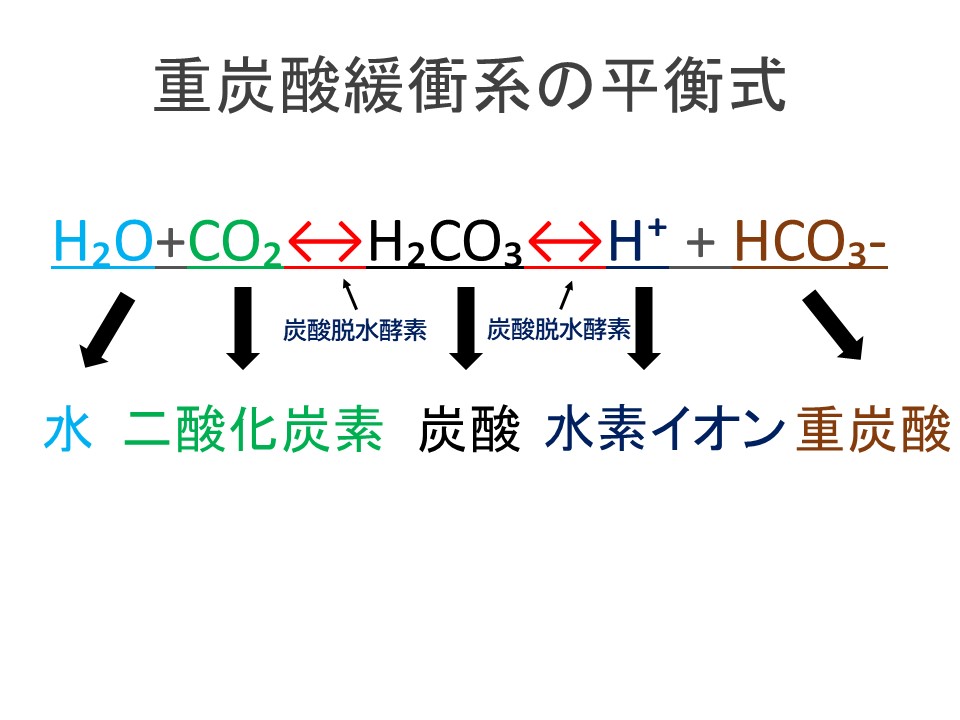
ら行われているが,多くは,炭酸イオンや重炭酸イオンの 解離平衡状態を対象にしている 2)。 ところで,二酸化炭素の水への溶解は水との相互作用と して調べる上で,水の中での二酸化炭素や炭酸イオンの存 在状態は非常に重要と考えられる。水の中での二酸化炭素 や炭酸イオンの存在状態 13 及びカリウムイオンに解離し、炭酸水素イオンは、式 1 のとおり、炭酸となった後、 14 酸化炭素 及び水を生成する。(参照2、8)概要書、1(別1) 15 16 式 1 ぶどう酒における炭酸水素イオンの反応 17 炭酸水素イオン(hco 3) + 水素イオン(h) 18 → 重炭酸緩衝液システム は、 炭酸 酸塩基恒常性 メカニズムです。>)、 重炭酸イオン (hco 3 )、および 二酸化炭素 (co 2 )は、 ph を維持するために 血液 および 十二指腸 、とりわけ、適切な 代謝 機能をサポートします。 炭酸アンヒドラーゼ によって触媒され、炭酸水素塩(co 2
酸と塩基 電離平衡
炭酸 イオン解離式
炭酸 イオン解離式-Hco3 ⇔ h + co3 2 ・・・(3) 炭酸水素イオンが炭酸イオンに解離する反応 ここで大事な点は、(2)(3)の式の右辺に水素イオン(h )が存在するということで、これらの関係 はphによって支配されています。アルカリ性に傾く(phが高くなる)ことはすなわち溶液中の水素(炭酸( ),炭酸水素イオン( )及び炭 酸イオン( )の間には式(1)に示す化学平 衡が成立している. (1) 全炭酸中の三つの物質の存在比は,水温,塩分及 びpH によって変動する(第1 図).海洋




気象庁 海洋の健康診断表 総合診断表 第2版
式としては,Royらの式(RoyetaL,1993)やMilleroの式(Millero,1995)がある。 (2-3)式と(2-4)'式の表現に従えば,全炭酸濃度αは,(2-8)式で表わされる。 GT= CO2*(aq)+ IHCO3一(aq)+ ICO32一(aq)1 (2-8)するので酸である.また,2段階に解離し,水素イオンを2個放出するので2価の酸で ある. 解答2 式(2-2)の係数a,b,c,d はすべて1とするので,濃度平衡定数,Kc =(CD) /(AB)と書ける.ここで,A=0100 mol/L,B= mol/L,C= 炭酸水素ナトリウムを水に溶かした際に生じる炭酸イオンの濃度は、次の1,2で表される平衡式により決まる。 1 h2co3⇔h +hco32 hco3⇔h +co32(1)炭酸水素ナトリウム水溶液では 2hco3⇔h2co3+co32 a a式の平衡も成り立つ。この平衡定数kを求めよ。
炭酸イオンの構造は正三角形であり、構造は右のように3 つの 構造式で表される。このような共鳴構造については以前にも紹 介した。 過炭酸塩 正式にはペルオキソ炭酸塩という。例えばペルオキソ炭酸ナトリウムNa 2 CO 4。 ペルオキソ炭酸は 電荷収支式、物質収支式を立てよ。ただし、水の解離反応は考えなくてよいものとする。 という問題(分析化学)についてです。 硝酸 hno3→h^ no3^電荷収支式(以下電) h^=no3^ 物質収支式(以下物) no3^=01mol/dm^3 亜硝酸 3hno2→2no 3h^ 電離式 (10選) 電離式を理解するには,これまでに学習した化学式やイオンを表す化学式が基本になります. 合わせてこちらの記事も参考にしてください. 中学生が学習する化学式についてまとめました.絶対に覚えたい化学式の他に,難関高校で問われる
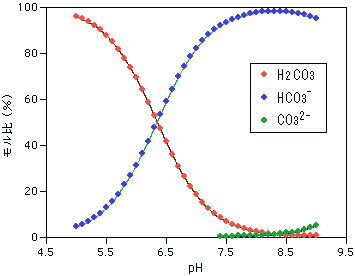
イオンの種類によって電荷の数が異なり、1価のイオンはNa 、K 、Cl、HCO 3 − など、2価のイオンはCa 2+ 、Mg 2+ 、HPO 4 2、SO 4 2などがあります。非電解質は、水に溶かしても解離しない(イオンにならない)もので、血液中に含まれるブドウ糖、脂肪、尿素などがあります。S62 炭酸塩水溶液のpH 炭酸水素イオンHCO 3 – は非常に弱い酸(pK a 約10)なので,炭酸水素ナトリ ウム水溶液中でHCO 3 – はほとんど解離していない. a すなわち,HCO 3 –/CO 3 2– >> 1であり,Henderson–Hasselbalchの式(式63)か炭酸は、海洋中では水素イオン(h + )が解離した炭酸水素イオン(hco 3 - )や炭酸イオン(co 3 2- )との間で式(2)や式(3)で表される反応により化学平衡の状態を保っている。 大気中の二酸化炭素が増えると、海水に溶け込む二酸化炭素も増え、式(1)と式(2)の反応が右に進んで




水溶液とイオン8 練習問題と積み上げプリント ラスカルのブログ




2 2 3 電離平衡
アルカリ性の水溶液になる電離式 赤字がよく出るもの ① 水酸化ナトリウムの電離 NaOH → Na⁺ + OH⁻ ② 水酸化バリウムの電離 Ba(OH)₂ → Ba²⁺ + 2OH⁻ ③ アンモニアが水に溶けたときの電離 NH₃ + H₂O → NH₄⁺ + OH⁻ ④ 水酸化カリウムの電離腎における重炭酸イオン生成 50~70 meq/日 不揮発性酸腎による重炭酸 イオン消費 50~70 meq/日 pco2 hco3 - 図 1 生体における酸の生成と肺および腎からの排出 ばれる。これらの分子が水という溶液のなかで存在すると きは,ha h++a-なる解離式で表わされる。塩基は, hco 3炭酸水素ナトリウム(重曹)は化学式nahco 3 であらわされる化合物で、体内でna とhco 3に解離する。 hco 3は重炭酸イオンと呼ばれ、酸を中和し
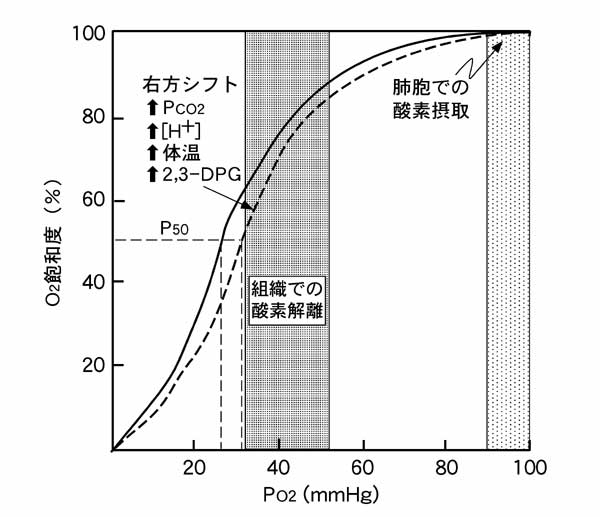



呼吸器系8 呼吸生理1



酸解離平衡と吸光度の変化
①②式より、加水分解度h=( € Kw 001Kb )になる。電離定数Kb=18×105であるとすると、溶 液のpHは、H=( 24×106 )より、pH=( 56 ) 問11 0mol/Lの炭酸ナトリウムのpHを求めよ。炭酸水素イオンの電離定数Ka2=48×1011であ25℃において、水のイオン積K w は10 -14 であることから、共役の関係にある酸および塩基の解離定数および解離指数においては、以下の式が成立する。 K a ×K b =K w =10 -14 pK a +pK b =pK w =14 2 分子形、イオン形の存在比とpHの関係 式①は,式③の両辺から 4 h 2 o を省略したものであり,また式②は,式④の両辺 から 5 h 2 o を省略したものである。 一般に,アルカリ金属とアルカリ土類金属のイオンを除く金属水和イオンは,水 溶液中で h を h 2 o に与えることができるので,すべて



102 97 解説 Yaku Tik 薬学まとめました
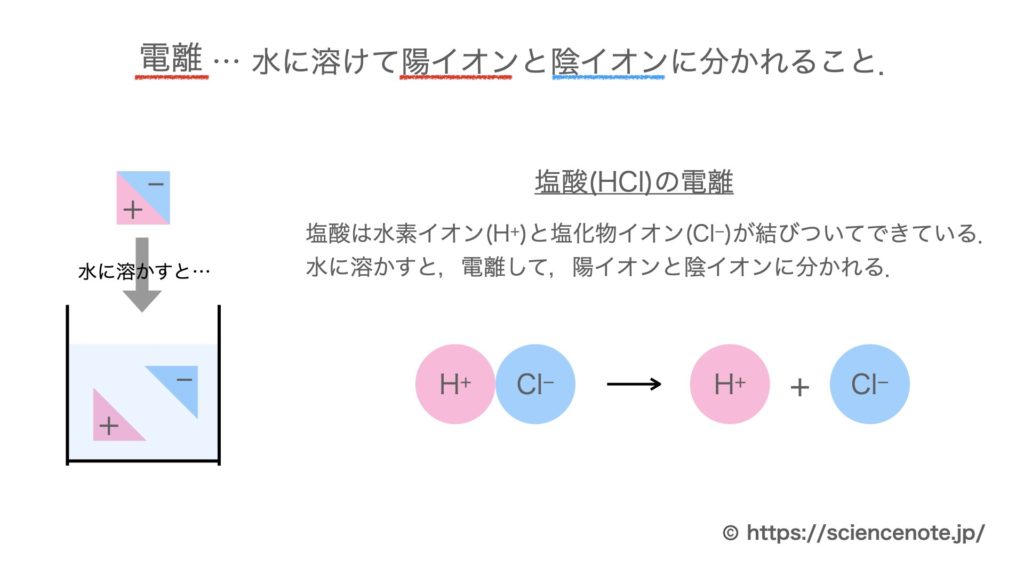



電離とは 電離式まとめ10選 中学化学 Hiromaru Note
その式を1)とします。 各成分のモル濃度を成分と記します。 (B) ・大気中の二酸化炭素が海水に溶けて、炭酸イオンまで解離する反応式を書き出してください。 ・水の解離平衡の反応式も書き出してください。 ・各反応(溶解平衡と解離平衡)について、質量作用の法則の式を書き出してくだPH 10炭酸塩緩衝溶液{02 mol/L炭酸ナトリウム溶液} <原理> 酸塩基指示薬(HX)の色の変化は、一般に次のような化学平衡に基づくものである。 HX ⇔ H X解離平衡の式から、水素イオン濃度が指示薬の酸解離定数 K I の値に近いとき、 pHの変動にともなって、共役酸・塩基の存在量の逆転がPHが高い場合はプロトンを供給する方向に進むので、炭酸水素イオン HCO3 が炭酸イオン CO32 とプロトンに分解され、炭酸イオン CO32 がカルシウムイオン Ca2 と結合して炭酸カルシウム CaCO3 になり沈殿します。




13 号 水棲動物の保存および輸送方法 Astamuse
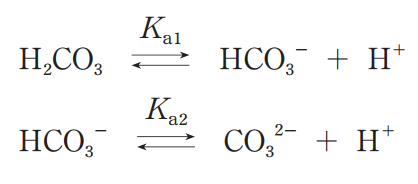



ヒトの体液は主に炭酸と炭酸水素イオンの濃度バランスにより Ph 7 4に維持されている Ph 7 3のアシドー
電離平衡の一段目のみの解離を考慮し,二段目は極めて小さいため無視できと仮定し,酸濃度が極端に低くない場合に HCO3- ≒ H3O+ ,酸濃度 C ≒ H2CO3 とすることで,一段目の電離平衡から H3O+ 2≒ C Ka1炭酸は、炭酸水素イオン(HCO 3)と炭酸イオン(CO 3 2)の2段階に解離します。これらを合わせた炭酸系物質のことを、全炭酸(Dissolved Inorganic Carbonate DIC)といいます。全炭酸(DIC)の濃度は式(1)で表されます。 DIC = HCO 3 CO 3 2 H 2 解離平衡は電解質が水に溶けているときの化学平衡。つまり解離定数は平衡定数の一種です。 しかし、このように視点を細かくしていくことで平衡について理解を深めることができます。 電解質の分類 電解質は水中で陽イオンと陰イオンに電離しますね。




14 号 変色麺の製造方法及び変色麺 Astamuse
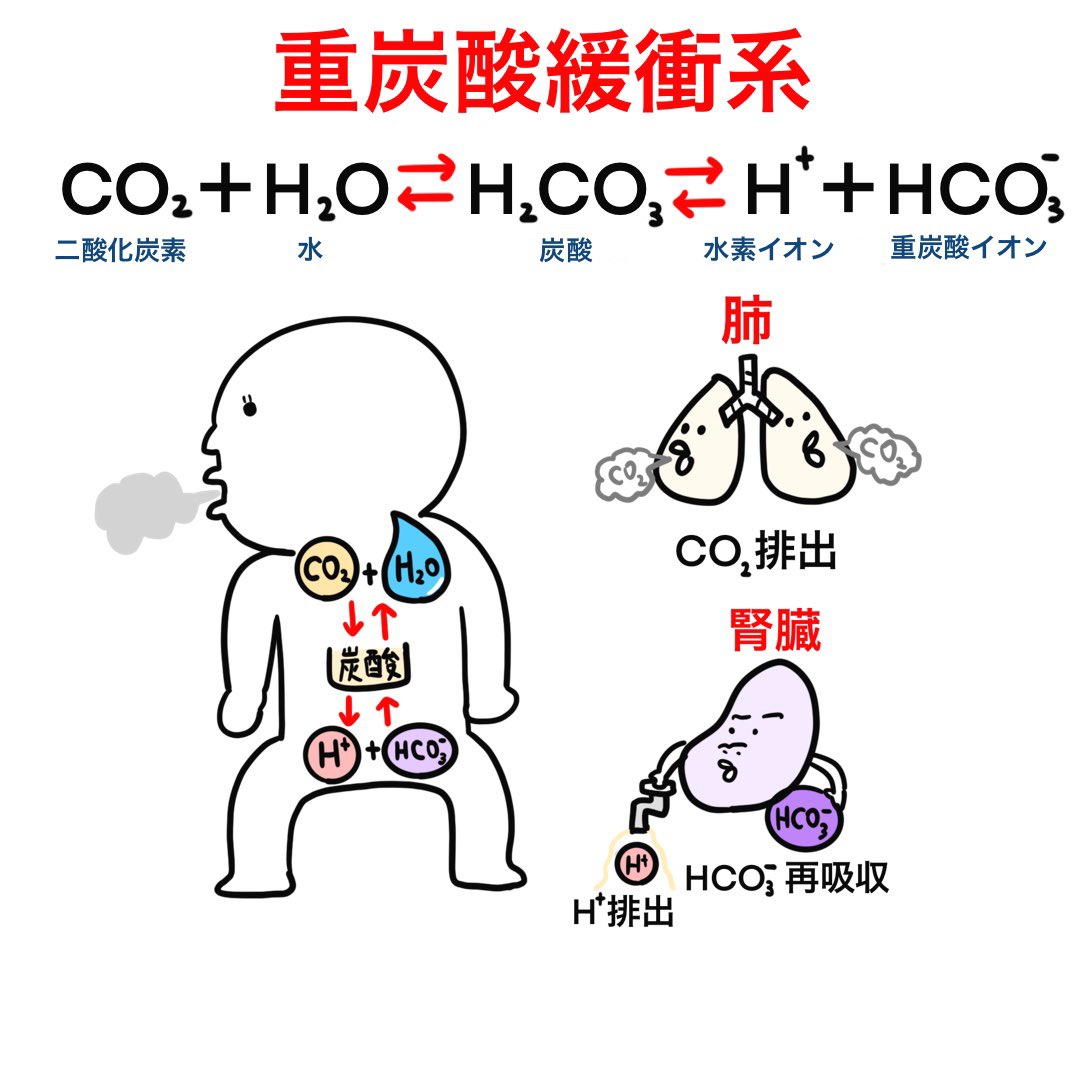



ゴロ 解剖生理イラスト イラストで分かる 重炭酸緩衝系 肺 二酸化炭素を排出してphを調節 腎臓 水素 イオンを排出 重炭酸イオンを再吸収してphを調節
(BCG)は弱酸であり,非解離分子の濃度(C H) と解離イオンの濃度(C I),pH の 3 者の関係は(1) 式(HendersonHasselbalch の式)で表される。 (1) -158 - 三 島・大 沢・山 田・北 岡 pH pK C a C I H = log 9 及びカリウムイオンに解離し、炭酸水素イオンは、式 1 のとおり、炭酸となった後、 10 酸化炭素 及び水を生成する。(参照2、8)概要書、1(別1) 11 12 式 1 ぶどう酒における炭酸水素イオンの反応 炭酸水素イオン(hco 3 13 ―) + 水素イオン(h+) 14 →となり,弱酸水溶液のヒドロニウムイオン量( H 3 O +),電離度(α),酸解離定数( Ka )の間に, H 3 O + = C 0 α ≒ ( C 0 Ka ) 1/2



温泉の科学5 5 1



1
反応式の各物質の係数比や,イオンの価数に注目して化学式を表すこと。各反応式はそれぞ れ次のようになる。 (1) 酸と塩基の反応である。 2ch 3coohca( oh) 2→ca( ch 3coo) 22h 2o (2) 塩と酸の反応である。石灰水にco 2 を吹き込むとcacoで炭酸水素イオンからギ酸イオンへの還元反応が進行した.また,ギ酸イオン生成量は添加水素量の1/2 乗 に比例し,反応容器表面に解離吸着した水素分子によって炭酸水素イオンが還元された.還元反応の初期段 階における反応速度式をdHCOONa/dt = NaHCO3 H2Ⅲ2 酸・塩基の電離と水素イオン濃度 Ⅲ21 弱酸 ex 酢酸 ch 3cooh 希薄水溶液( 01mol/l 以下)中では、一部が解離し、大部分は分子状で存在 ch 3cooh ⇄ch 3coo −+h+ 化学平衡の法則より、 ch 3coo −h ch 3cooh =ka



7 酸塩基平衡における 重炭酸緩衝系 とは何か



3
両性電解質水溶液の水素イオン濃度 15 年8 月5 日 炭酸水素ナトリウム水溶液中では、nahco3 は、na とhco 3 に完全に電離している。 ここで、 hco 3 は、 hco 3 ⇀↽ h hco 3 (1) と電離して、水素イオンを放出できる(酸として働く) が、hco 3B:塩基解離定数 K w:水のイオン 解離平衡 酸 分子式 Ka / mol dm3 pK a 塩酸 HCl 硝酸 HNO3 硫酸 H2SO4* 0010 (Ka2) 199 炭酸 H2CO3* 745×10 (K a1) 635 1147×10 (Ka2) 1033 ギ酸 HCOOHス電極水素イオン濃度計で測定し,又 炭酸の解離定数 を,PK1=10・2,PK2=6・4と して計算式から求めた水 素イオン濃度の計算値をTable1に 示した



炭酸の化学式と電離式を教えていただきたいです 以下のようにな Yahoo 知恵袋




第4話 溶離液組成による分離の調節 ご隠居達のic四方山話 よもやまばなし シーズン3 メトローム
ただし炭酸のpKa1=63、pKa2=104である。 1、この溶液の質量均衡則と電荷均衡則を書いてください。 2、炭酸の酸解離定数Ka2の式を書いてください。 3、炭酸イオンの塩基解離定数Kb1の式を書き、pKb1の数値を求めてください。 すみませんが途中の過程や解説も3イオン化と解離の違いは何ですか 主な違いの比較 キーワード:原子、解離、解離定数、電子、イオン化合物、イオン化、イオン化エネルギー、イオン対、放射線、ラジカル イオン化とは イオン化は、原子または分子が正または負の電荷を帯びるプロセスです。これは、原子または分子血液は重炭酸を主なイオンとする緩衝液と捉え、古典的アプローチでは 血液の酸塩基平衡状態を pH=61 log(HCO3/(003xP CO 2 ) ) ( HendersonHasselbalchの式)
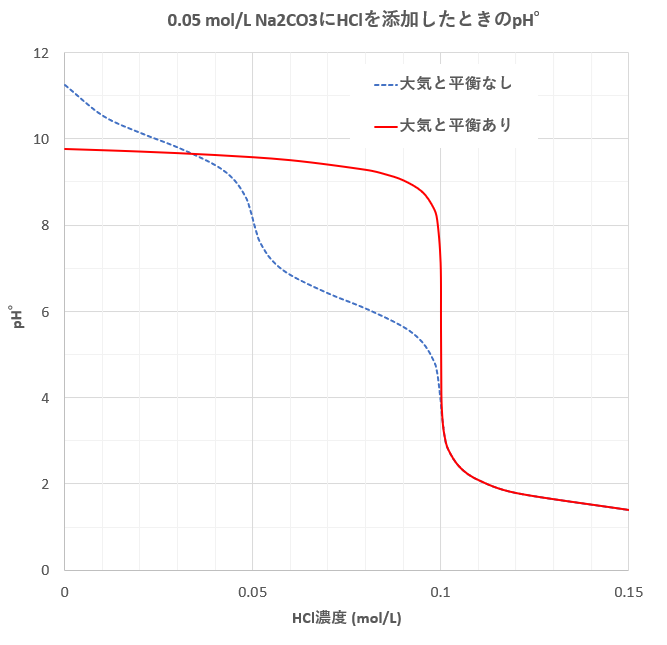



二酸化炭素の溶解と酸塩基平衡 1 大気との平衡 滴定曲線 溶解度などーエクセルを用いて
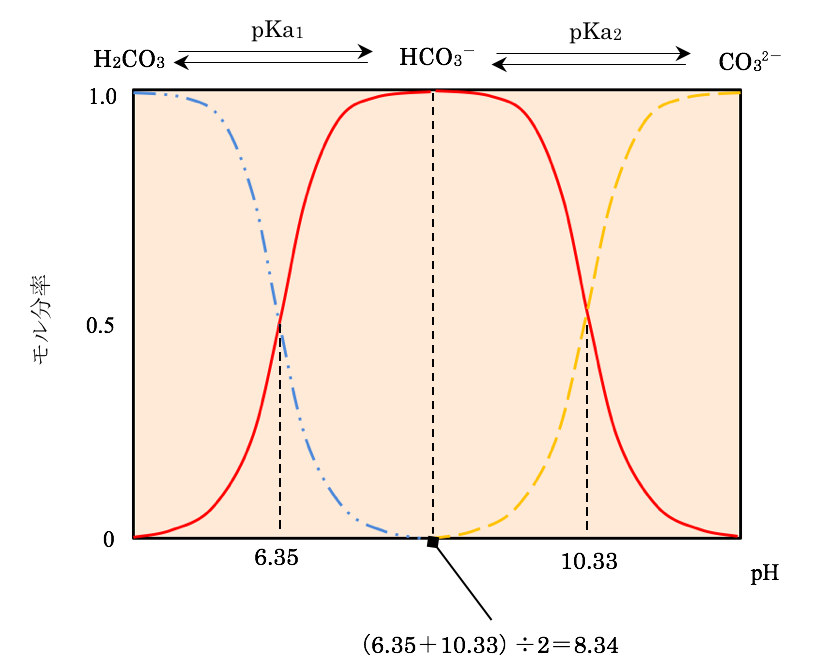



Phの測定 溶液のph Yakugaku Lab
Na2CO3 水溶液の水素イオン濃度 15 年2 月16 日 ある濃度(c mol/Lとしよう)のNa2CO3 水溶液がある。 この水溶液の水素イオン濃度Hを求めるに はどうしたらよいのであろう。ここで、二酸化炭素(炭酸)の第1電離定数(第1酸解離定数)K1 と第2電 離定数(第2酸解離定数)K2 水と二酸化炭素から炭酸のできる反応式は H 2 O(l) CO 2 (aq) ⇄ H 2 CO 3 ですが、文献では、その平衡定数は25℃で17×103 だそうです(J Phys Chem 1969, 73 炭酸ナトリウムは炭酸水素ナトリウムよりも塩基性が強いですが、 その理由として、 (1)H2CO3 ⇔ H () HCO3 () (2)HCO3 () ⇔ H () CO3 (2) ※イオンの価数は ( )で表しています。 「(2)の平衡は(1)の平衡よりもずっと左に偏っているので、 CO3 (2) は HCO3



スズケンdiアワー 平成14年7月11日放送内容より スズケン Di実例集 137 昭和大学病院 薬剤部 竹ノ内 敏孝 血漿重炭酸イオン濃度の算出法 本日は 酸 塩基代謝障害と血漿重炭酸イオン濃度の算出法についてお話させていただきます まず 酸 塩基




2 2 3 電離平衡
代謝によって産生されたco2は、水と反応して炭酸(h2co3)となり、炭酸は解離して、水素イオン(h)と重炭酸イオン(hco3)になる。すなわち、co2 + h2o ⇔ h2co3 ⇔h + hco3 という反応が発生し、平衡する。 赤血球によるco2の運搬



がんのアルカリ療法
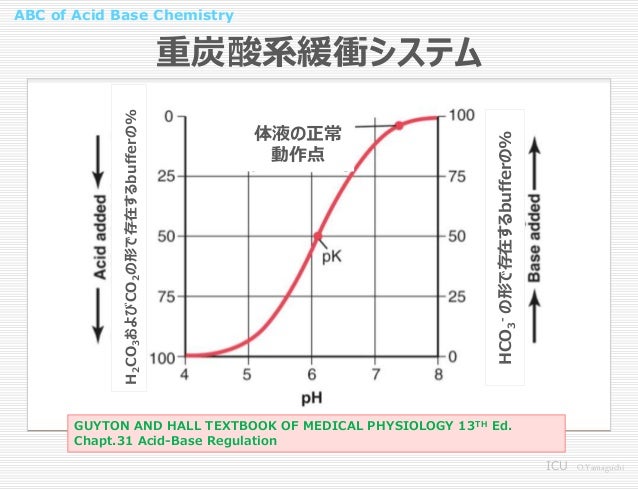



Abc Of Acid Base Chemistry




Phの測定 溶液のph Yakugaku Lab
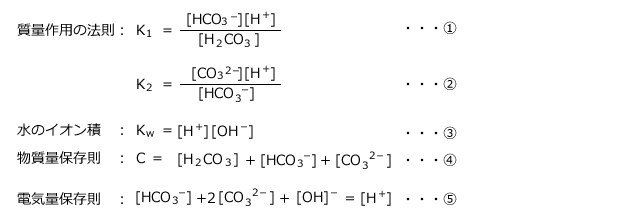



化学講座 第56回 化学反応速度 弱酸 弱塩基の電離 私立 国公立大学医学部に入ろう ドットコム




炭酸の電離式を教えてください Clearnote




酸塩基平衡 後編 重炭酸緩衝系とは Youtube




第4話 溶離液組成による分離の調節 ご隠居達のic四方山話 よもやまばなし シーズン3 メトローム




炭酸 Wikipedia




体液のph 水素イオン濃度 はどれくらい 看護roo カンゴルー




炭酸ナトリウムの二段階滴定について 化学がちょっとだけ好きな社労士




Ph 沸騰させた水 Fame Bio Diesel Fuel f Teacup ブログ Autopage




電離平衡




化学講座 第56回 化学反応速度 弱酸 弱塩基の電離 私立 国公立大学医学部に入ろう ドットコム



Http Plaza Umin Ac Jp Histsite 5resprtxt Pdf



酸と塩基 電離平衡




化学講座 第56回 化学反応速度 弱酸 弱塩基の電離 私立 国公立大学医学部に入ろう ドットコム




1995 1072号 連続式イオンリッチ水生成方法および装置 Astamuse




なぜクエン酸は酸性で 重曹はアルカリ性なのか 両者の意外な関係とは 日本霜降社



Ph曲線とアルカリ度 水浄化フォーラム 科学と技術



Ooki Dic 2 アルカリ度と炭酸成分



Ph曲線とアルカリ度 水浄化フォーラム 科学と技術



簡単に理解できる酸塩基平衡 認定看護師のブログ 働く人を支える アイエスイノベーション



酸塩基平衡



Http Www Fumi Theory Com Img Jf Ph Pdf




11 号 炭酸ガス処理装置及び炭酸ガスの処理方法 Astamuse



重炭酸湯とは Mybathtime マイバスタイム




アンモニア Nh3 の電離式を教えてください Clearnote



酸と塩基 電離平衡




気象庁 海洋の健康診断表 総合診断表 第2版



酸と塩基 電離平衡




気象庁 海洋の健康診断表 総合診断表 第2版
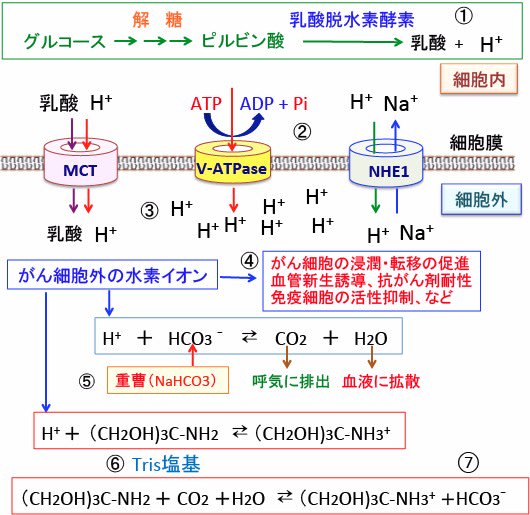



666 がんのアルカリ療法 その3 重曹 重炭酸ナトリウム とトリス塩基 漢方がん治療 を考える




Ph 沸騰させた水 Fame Bio Diesel Fuel f Teacup ブログ Autopage
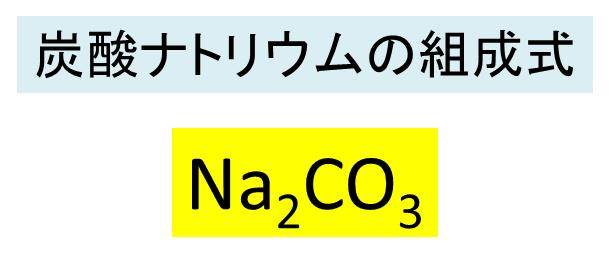



炭酸ナトリウム Na2co3 の化学式 分子式 構造式 電子式 イオン式 分子量は 炭酸ナトリウムの工業的製法



Ph曲線とアルカリ度 水浄化フォーラム 科学と技術




気象庁 海洋の健康診断表 総合診断表 第2版
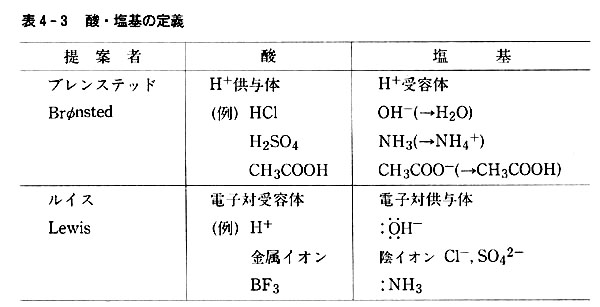



4 水と酸 塩基




炭酸水素ナトリウムの水溶液が塩基性なのはなぜ 化学反応式を解説 地学博士のサイエンス教室 グラニット
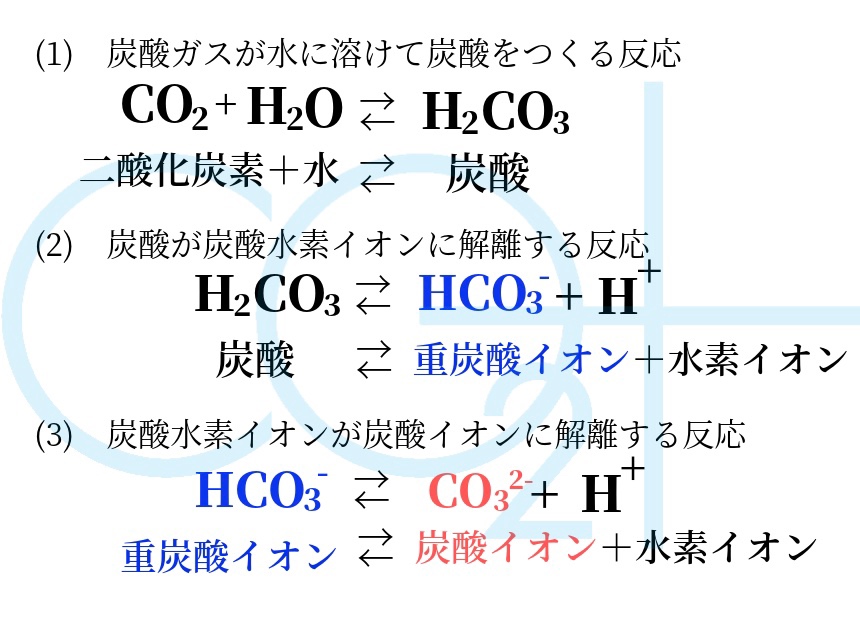



誤解していませんか 重炭酸浴と炭酸浴の大きな違い



質問に答えることができなかった ため息 2ばかりのブログ
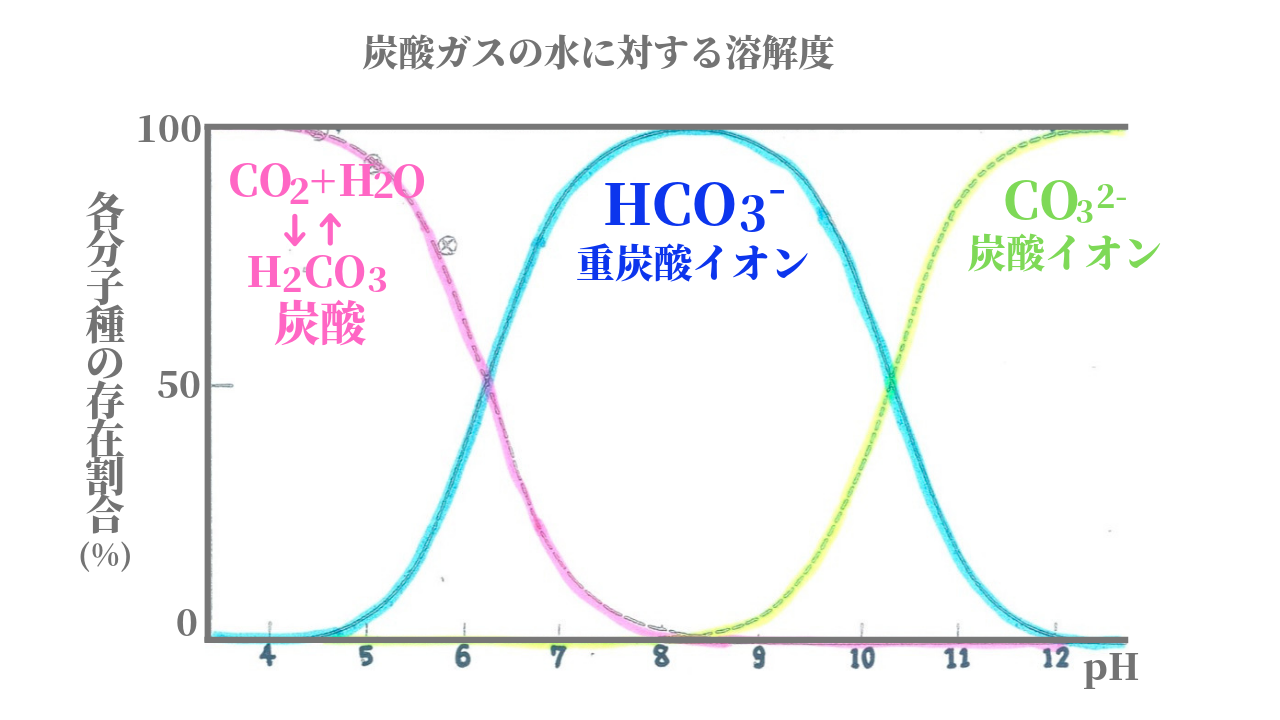



誤解していませんか 重炭酸浴と炭酸浴の大きな違い




Excel イオン式 電離式の練習用教材 中学理科ポイントまとめと整理 オンラインショップ
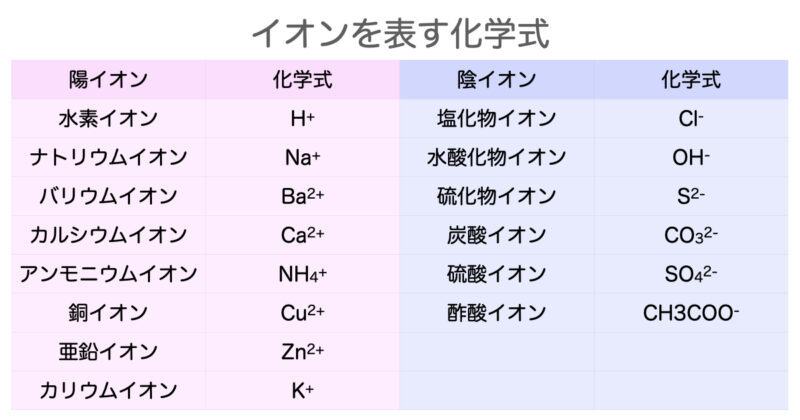



これだけは覚えたいイオンを表す化学式 イオン式 一覧 Hiromaru Note



2 2 3 電離平衡



3



中学生です 炭酸水の電離式と その理由を教えてください お Yahoo 知恵袋
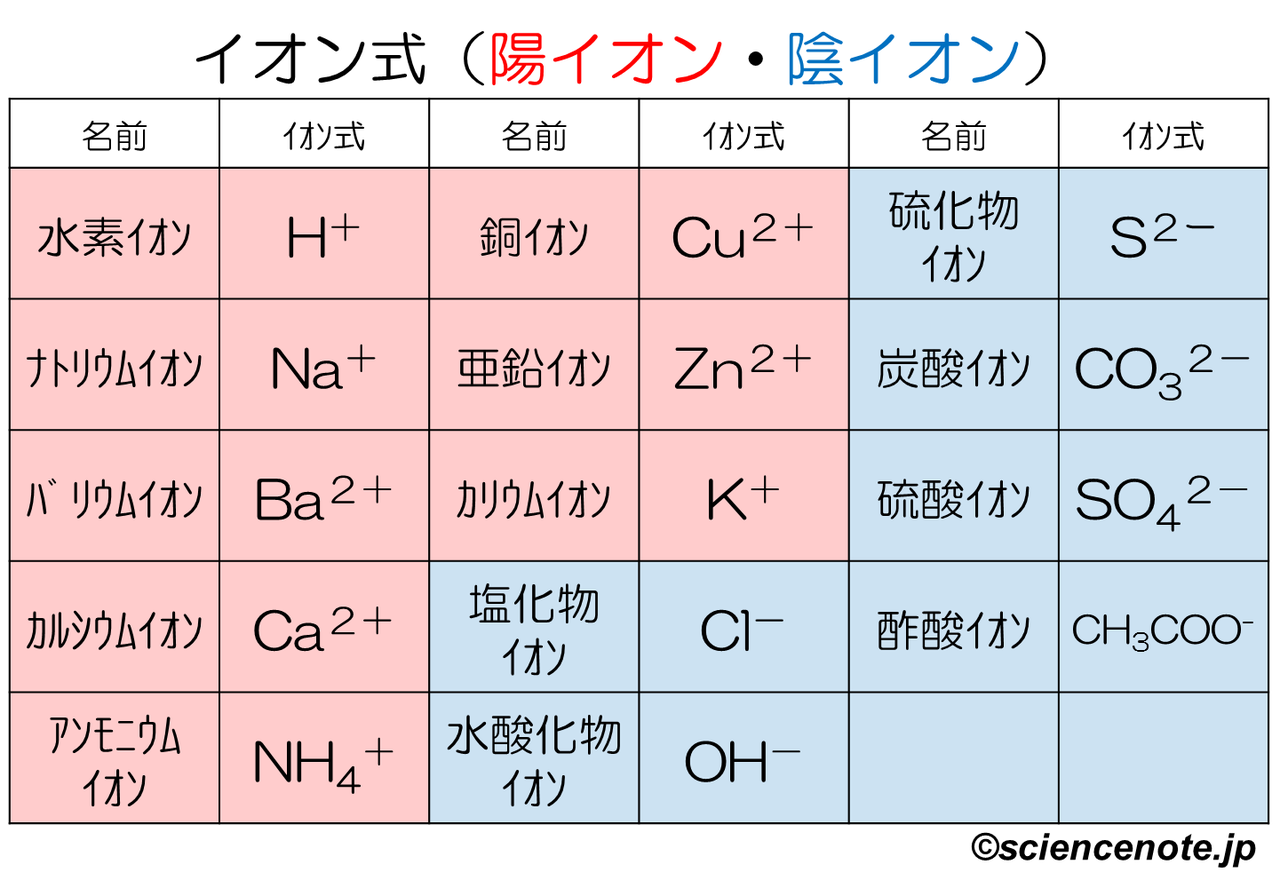



これだけは覚えたいイオンを表す化学式 イオン式 一覧 Hiromaru Note
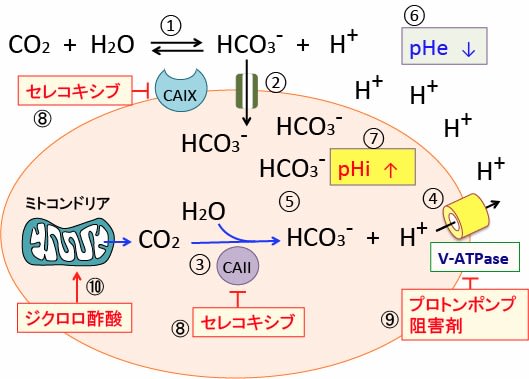



666 がんのアルカリ療法 その3 重曹 重炭酸ナトリウム とトリス塩基 漢方がん治療 を考える



Http Data Jci Net Or Jp Data Pdf 37 037 01 1259 Pdf



Www Cps Jp Org Cps Pub Seminar Fy11 11 12 06 Kitamura Pub 1116 Kitamura 02 Pdf
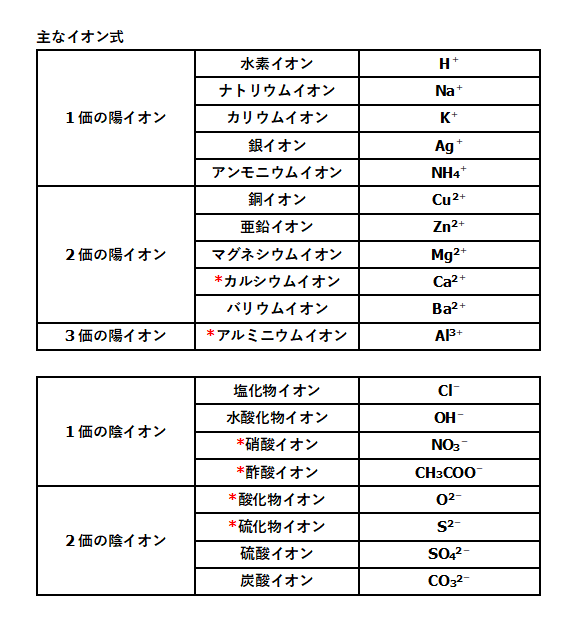



イオン式 電離式まとめ 中学理科 ポイントまとめと整理



Http Armt Net Images Files Pdf Files Ivp News Pdf Article12 Ivpnews 12 01 01 Pdf



1
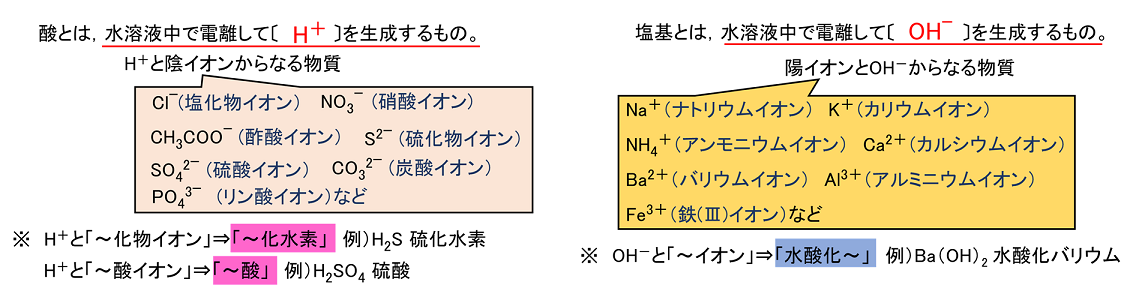



酸と塩基




化学講座 第56回 化学反応速度 弱酸 弱塩基の電離 私立 国公立大学医学部に入ろう ドットコム




Wo09 号 ハイドロタルサイト様物質の層間イオン置換方法 再生方法および層間イオン置換装置 Astamuse
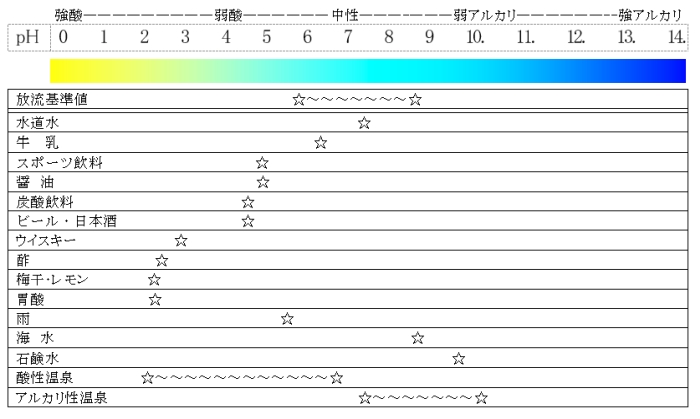



Phとは 株式会社トーケミ




炭酸水素ナトリウムを水に溶かした際に生じる炭酸イオンの濃度は 次の 化学 教えて Goo



7 酸塩基平衡における 重炭酸緩衝系 とは何か



Http Www Fumi Theory Com Img Jf Ph Pdf
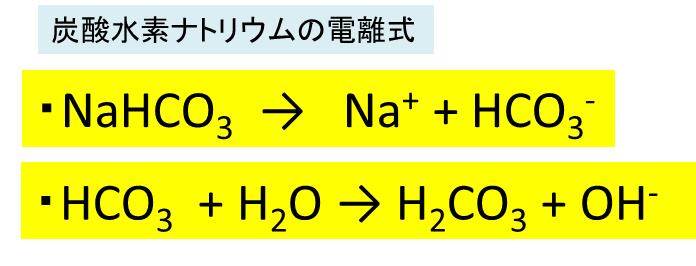



炭酸水素ナトリウム Nahco3 の化学式 分子式 構造式 電子式 イオン式 分子量は 炭酸ナトリウムの工業的製法



Ph曲線とアルカリ度 水浄化フォーラム 科学と技術




Excel イオン式 電離式の練習用教材 中学理科ポイントまとめと整理 オンラインショップ



西村 1991 による




炭酸ナトリウム Wikipedia




補講 炭酸の平衡 炭酸水素ナトリウムのph Youtube




炭酸でよく見ますが 電離度a Clearnote




炭酸ナトリウム Na2co3 の化学式 分子式 構造式 電子式 イオン式 分子量は 炭酸ナトリウムの工業的製法




Excel イオン式 電離式の練習用教材 中学理科ポイントまとめと整理 オンラインショップ



Www Jma Go Jp Jma Kishou Books Sokkou Kaiyou Vols081 Pdf



Ooki Dic 2 海水中での炭酸成分の解離平衡




電離平衡



水素イオン濃度




Excel イオン式 電離式の練習用教材 中学理科ポイントまとめと整理 オンラインショップ




至急お願いします Clearnote




イオン式 電離式まとめ 中学理科 ポイントまとめと整理



3回生実験のこと 実験の基礎4 3
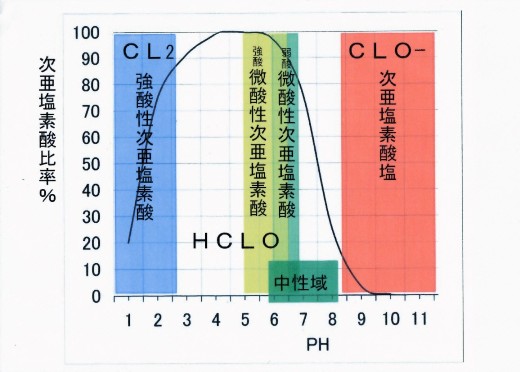



次亜塩素酸水



4 酸塩基平衡 塩基 とは 重炭酸イオンのことである




高校理論化学 極端に希薄な強酸水溶液のph 受験の月



7 酸塩基平衡における 重炭酸緩衝系 とは何か




Phと酸解離定数pkaの関係 バッファーの基礎知識 M Hub エムハブ
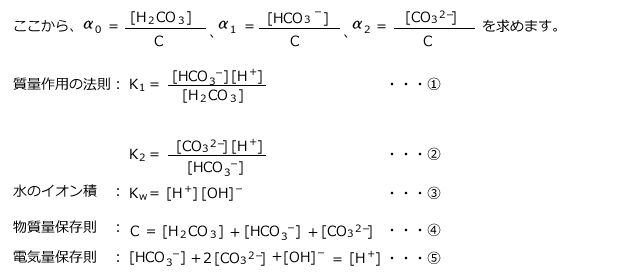



化学講座 第56回 化学反応速度 弱酸 弱塩基の電離 私立 国公立大学医学部に入ろう ドットコム
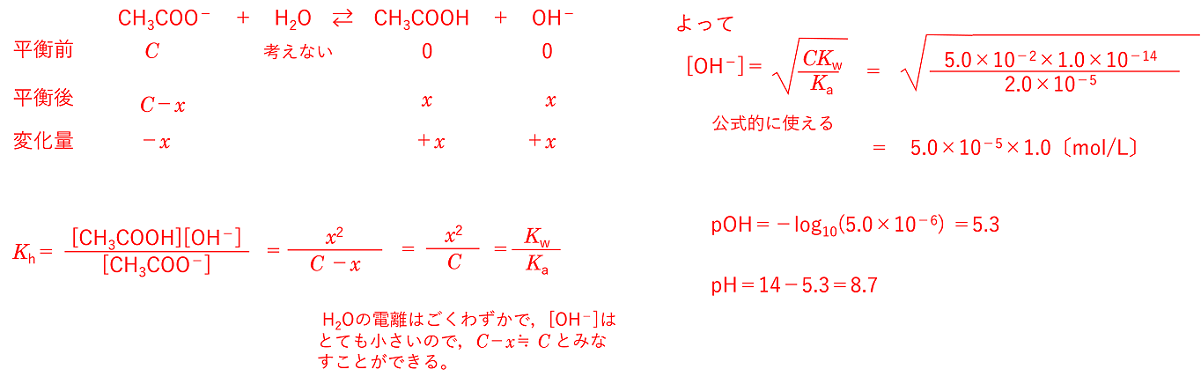



電離平衡
コメント
コメントを投稿